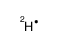sodium deuteride
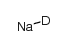
sodium deuteride结构式

|
常用名 | sodium deuteride | 英文名 | sodium deuteride |
|---|---|---|---|---|
| CAS号 | 15780-28-6 | 分子量 | 25.00390 | |
| 密度 | N/A | 沸点 | N/A | |
| 分子式 | DNa | 熔点 | N/A | |
| MSDS | N/A | 闪点 | N/A |
| 英文名 | sodium deuteride |
|---|---|
| 英文别名 | 更多 |
| 分子式 | DNa |
|---|---|
| 分子量 | 25.00390 |
| 精确质量 | 25.00390 |
| LogP | 0.11250 |
| 更多 | 1.性质:本品为灰白色粉末,易吸湿. |
|
~% 
sodium deuteride 15780-28-6 |
| 文献:Hackspill, L.; Borocco, A. Bull. Soc. Chim. France (5), 1939 , vol. 6, p. 91 - 103 Full Text Show Details Hackspill, L.; Borocco, A. Comptes Rendus Hebdomadaires des Seances de l'Academie des Sciences, 1937 , vol. 204, p. 1475 - 1477 |
| sodium deuteride上游产品 2 | |
|---|---|
| sodium deuteride下游产品 0 | |
本品系仿照氘化锂和氢化钠的制备方法由单质钠和氘气直接化合而成。
图Ⅰ-13由D2O和Na取制D2
1—玻璃反应器;2—玻璃装置;3,4—活栓首先要制得纯的钠和氘气,金属钠须真空蒸馏并多次提纯,而氘气则由高纯重水和金属钠反应制得。可以得到纯度达99.8%的氘化钠。
氘气的提纯按图Ⅰ-13的装置及下述反应进行:
2D2O+2NaD2+2NaOD
在装置的玻璃反应器的1瓶中有一铝坩埚,盛过量金属钠。隔绝空气,将准备分解用的D2O装入2中。用液态空气将2冷却后,打开活栓3和4,仔细地抽真空。然后关闭活栓4,用液态空气将1冷却使D2O慢慢蒸馏到Na上来。此后将在350℃加热数小时,使反应完全。打开活栓4之后,把瓶中发生的D2打入一装有脱过气的活性炭并排空的容器中,于-185℃下放置。当Na是第一次使用时,制得的D2中还含有少许H2(系溶于金属Na中杂带的NaOH所生成)。只有仍用此同一块Na,第二次分解,方可制得纯D2,其杂质含量少于0.2%。其纯度用测量热导率方法检定。
金属Na用前应在二甲苯中重新熔融数次以除去沾附的难挥发烃属化合物,并尽可能除去氧化物。在氩氛中将表面光洁的Na装在制备碱金属氢化物的常用装置(图Ⅰ-7)的舟中,将反应器抽空,并充以氘气,加热。温度徐徐升到750℃,待装置中的压力保持不变(至少半天),确认氘化钠生成完全。俟充分冷却后,在惰性气氛保护下,用焊在长玻璃棒上的小铂铲将氘化钠取出。
| EINECS 239-875-0 |
| Sodium hydride-d1 |
| SODIUM HYDRIDE {609.1.6} |
| (2H)Hydridesodium |
| Natriumdeuterid |