硫霉素
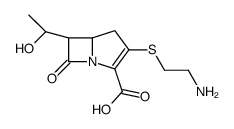
硫霉素结构式

|
常用名 | 硫霉素 | 英文名 | Thienamycin |
|---|---|---|---|---|
| CAS号 | 59995-64-1 | 分子量 | 272.32100 | |
| 密度 | 1.5g/cm3 | 沸点 | 514ºC at 760 mmHg | |
| 分子式 | C11H16N2O4S | 熔点 | N/A | |
| MSDS | N/A | 闪点 | 264.7ºC |
硫霉素用途第一个天然碳青霉烯类抗生素,具广谱、高效、对细菌β-内酰胺酶稳定等特点。但化学性质不稳定,难以直接应用于临床。 |
| 中文名 | 硫霉素 |
|---|---|
| 英文名 | (5R,6S)-3-(2-aminoethylsulfanyl)-6-[(1R)-1-hydroxyethyl]-7-oxo-1-azabicyclo[3.2.0]hept-2-ene-2-carboxylic acid |
| 中文别名 | 亚胺培南 |
| 英文别名 | 更多 |
| 密度 | 1.5g/cm3 |
|---|---|
| 沸点 | 514ºC at 760 mmHg |
| 分子式 | C11H16N2O4S |
| 分子量 | 272.32100 |
| 闪点 | 264.7ºC |
| 精确质量 | 272.08300 |
| PSA | 129.16000 |
| LogP | 0.22420 |
| 折射率 | 1.662 |
| 分子结构 | 1、 摩尔折射率:67.10 2、 摩尔体积(cm3/mol):181.1 3、 等张比容(90.2K):538.4 4、 表面张力(dyne/cm):77.9 5、 极化率(10-24cm3):26.60 |
| 更多 | 1.性状:白色固体,有引湿性。 2.溶解度:易溶于水,微溶于甲醇。 3.比旋光度:[α]D27+82.7°(C=1.0,水)。 4.UV最大吸收(水,Ph=4.8):296.5nm(ε7900);(Ph=2):309nm;(Ph=12):300.5nm。 |
方法1:发酵法。
一、种子培养
(1)往250ml装有折流板的锥形瓶中,移入50ml无菌溶媒A,在无菌条件下,将一试管冻干的Streptomyces cattleya菌种悬浮于该溶液。溶媒A的组成如下:自溶酵母10.0g,葡萄糖10.0g,磷酸盐缓冲液2.0ml,MgSO4?7H2O0.05g,蒸馏水1000ml,并用氢氧化钠调pH值至6.5。
(2)该培养瓶在28℃振荡(220r/min)48h。在无菌条件下,移出40ml该种子培养液,并和40ml无菌的20%(V/V)乙二醇混合。将2ml该混合液用吸移管移至无菌的管瓶中,冷冻并保存在液氮中。
(3)往250ml装有折流板的锥形瓶中,移入50ml溶媒A,再植入上面冷冻管瓶中的内容物。该种子瓶于28℃下振荡(160r/min)培育24h。
(4)往2L装有折流板的锥形瓶中,移入500ml溶媒A,植入10ml上面种子瓶的培养液。在28℃下振荡(160r/min)培育24h。
(5)往756L不锈钢发酵器中,移入67L溶媒A,植入1000ml(4)中得到的种子液。在28℃下搅拌(130r/in)和充气(0.283rn3/min)24h。如需要.可加入不超过0.1%的聚乙二醇2000作为消泡剂。
二、发酵
往5670L不锈钢发酵器中,移入4082L溶媒E,植入453L(5)中得到的液体。在24℃下搅拌(70r/min)和充空气(54.3cfm)144h。如需要,可加入不超过0.1%的聚乙二醇2000作为消泡剂。溶媒E的组成如下:西瑞糖(cerelose)25.0g,玉米浸液(湿)15.0g,酒糟10.0g,药用棉子液5.0g,CoCl2?6H2O0.01g,CaCO3 3.0g(pH值调节后),聚乙二醇2000 0.25%,自来水1000ml;用氢氧化钠调pH值为7.3。
三、分离和提取
(1)用4%(W/V)的助滤剂来过滤得到的4082L发酵液。往滤液中加入12g乙二胺四乙酸的钠盐,冷至6℃。保持在613,将pH值调至4.5±0.2。在48L/min的速率,用480L 20~50μm的Dowex 50×4 Na+来吸附该冷滤液。用480L去离子水来洗该吸附剂,然后用2%吡啶水溶液,以24L/min的速度来洗脱。收集3份洗脱液,各为300L、520L和240L,各含4%、16%和6%的活性物质。把第二份洗脱液浓缩至48L,并调至pH=7。
(2)该48L的浓缩液调至pH=7.3,用76L 50--100μm的Dowex 1×2来吸附,流出速度为7.6L/min。用去离子水在同样的速度下进行洗脱,收集4份洗脱液,各为48L、48L、70L和48L,并调pH值为7。鉴定得出70L洗脱液中含有68%的用于吸附的活性物质。把该洗脱液浓缩至18L,调pH值为7.0,冻干后得99g产品,310U/mg。
(3)10g该冻干固体溶于0.1mol/L 2,6-二甲基吡啶乙酸盐的缓冲液(PH=6.3)中。再用乙酸调至pH=6.3,用7.6 X 142cm的Dowex 50 X 8(200~400μm)的柱子进行层析,洗脱液为0.1mol/L的缓冲液,洗脱速度为25ml/min。收集第一份3L、200份20ml的流出液。合并第80份至第136份的流出液,用590ml去离子水稀释,得1760ml液体。该流体含62%用于层析的活性物质。
(4)上述得到的1760ml液体进行冻干。冻干得到的固体溶于约27ml0.1mol/L2,6-二甲基吡啶乙酸盐(pH=7.0)。用Bio-Gel P-2(200~400μm)5×112cm的柱子来层析,洗脱液为相同的缓冲液,速度为10ml/min。收集105份各20ml的流出液。经鉴定,合并第75份至第80份的流出液。经冻干得90mg硫霉素,10000U/mg。
方法2:合成法可以青霉素等为原料,可参见KaradyS,amato J S,Reamer R A and Weinstock L M.Stereospecific conversion of Penicillin to Thienamycin.J A C S,1981,103(22):6765~6767;Salzmann T,Ratcliffe R W,ChristensenB Gand Bouffard FA.A stereocontrolled synthesisof(+)-Thienamycin.J A C S,1980,102(19):6161--6163;Kametani T,Huang S P,Nakayama A and Hon.Da T.Further studies on the synthesis of Thienamycin:a facile and stereoseleetive synthesisof a bicyclicβ-keto ester by 1,3一dipolar cycloaddition.J Org Chin, 1982,47(12):2328--2331。
| (+)-thienamycin |


