瑞德西韦临床有效性如何判别?
发布时间:2020-02-11 12:43:32 编辑作者:华碧盛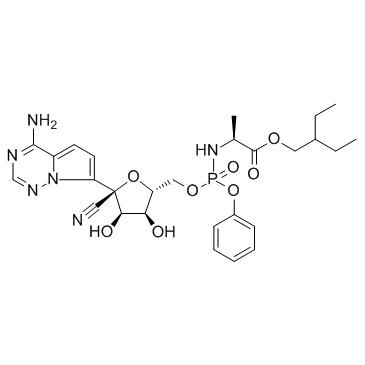
图片:瑞德西韦结构式
瑞德西韦的临床研究已经武汉金银潭医院启动!瑞德西韦(Re m di si vir)因其英文谐音也被冠以“人民的希望”的美誉,那么,它的效果究竟如何呢?
据《健康报》报道,试验组患者在标准治疗方案的基础上,接受首剂瑞德西韦200mg静脉点滴,随后连续9天每日100mg静脉点滴;对照组患者接受标准治疗和相同剂量安慰剂治疗。两部分临床试验均有严格的纳入/排除标准,入组患者将根据起病时间或病情严重程度,被分层随机分配至试验组和对照组,分配结果对受试者、医疗人员、试验工作人员均设盲。在入排标准方面,参加临床试验的病人的基线基本一致,否则会对临床研究结果产生干扰。
在疗效指标方面,分为主要结果指标和次要结果指标,时间窗为28天。
在主要结果指标中,临床恢复时间方面,从开始治疗(瑞德西韦或安慰剂)到发热、呼吸频率、血氧饱和度转为正常和咳嗽缓解,持续至少72小时。
发热方面,患者腋温≤36.6°C,或口温≤37.2 °C,或肛温或耳温≤37.8°C;
呼吸频率方面,在室内空气下,该指标≤24次/分;
血氧饱和度方面,在室内空气下,该指标>94%;
咳嗽程度方面,按“重度/中度/轻度/无”分级,患者咳嗽程度需达到轻度或无。
次要结果指标主要包括全因死亡、呼吸加重的发生频率、退热时间、呼吸困难转为轻度或无呼吸困难的时间、需要吸氧或无创通气的频率、上呼吸道样本2019-nCoV RT-PCR检测转为阴性的时间、上呼吸道样本中2019-nCoV病毒载量减少、需要机械通气的频率、严重不良事件的发生频率几方面,其时间窗也为28天。
该药此前临床研究证实了其安全性,不良反应主要是肾毒性,试验方案也详细规定了不良反应的处理方法。在临床试验操作上,由于患者全是住院环境,不需要招募入组,可最大限度的节省临床试验的开展时间。本次试验的观察时间为28天,如果患者在28天内出院,到28天的时候再来随访。为保证试验质量,从官网公布渠道来看,提供临床研究合同服务的CRO是在临床试验领域有着丰富经验的泰格医药公司。
参考资料:微博,武汉大学人民医院,研发客,化学科讯
据《健康报》报道,试验组患者在标准治疗方案的基础上,接受首剂瑞德西韦200mg静脉点滴,随后连续9天每日100mg静脉点滴;对照组患者接受标准治疗和相同剂量安慰剂治疗。两部分临床试验均有严格的纳入/排除标准,入组患者将根据起病时间或病情严重程度,被分层随机分配至试验组和对照组,分配结果对受试者、医疗人员、试验工作人员均设盲。在入排标准方面,参加临床试验的病人的基线基本一致,否则会对临床研究结果产生干扰。

在疗效指标方面,分为主要结果指标和次要结果指标,时间窗为28天。
在主要结果指标中,临床恢复时间方面,从开始治疗(瑞德西韦或安慰剂)到发热、呼吸频率、血氧饱和度转为正常和咳嗽缓解,持续至少72小时。
发热方面,患者腋温≤36.6°C,或口温≤37.2 °C,或肛温或耳温≤37.8°C;
呼吸频率方面,在室内空气下,该指标≤24次/分;
血氧饱和度方面,在室内空气下,该指标>94%;
咳嗽程度方面,按“重度/中度/轻度/无”分级,患者咳嗽程度需达到轻度或无。
次要结果指标主要包括全因死亡、呼吸加重的发生频率、退热时间、呼吸困难转为轻度或无呼吸困难的时间、需要吸氧或无创通气的频率、上呼吸道样本2019-nCoV RT-PCR检测转为阴性的时间、上呼吸道样本中2019-nCoV病毒载量减少、需要机械通气的频率、严重不良事件的发生频率几方面,其时间窗也为28天。
该药此前临床研究证实了其安全性,不良反应主要是肾毒性,试验方案也详细规定了不良反应的处理方法。在临床试验操作上,由于患者全是住院环境,不需要招募入组,可最大限度的节省临床试验的开展时间。本次试验的观察时间为28天,如果患者在28天内出院,到28天的时候再来随访。为保证试验质量,从官网公布渠道来看,提供临床研究合同服务的CRO是在临床试验领域有着丰富经验的泰格医药公司。
参考资料:微博,武汉大学人民医院,研发客,化学科讯
相关化合物:瑞德西韦
上一篇:69篇新冠病毒论文合集
版权声明:本站内容注明授权来源,任何转载需获得来源方的许可!若未特别注明出处,本文版权属于化源网,未经许可,谢绝转载!对未经许可擅自使用者,本公司保留追究其法律责任的权利。
免责声明:部分文章信息来源于网络以及网友投稿,我们会尽可能注明出处,但不排除来源不明的情况。本网站只负责对文章进行整理、排版、编辑,是出于传递更多信息之目的,并不意味着赞同其观点或证实其内容的真实性,如本站文章和转稿涉及版权等问题,请作者在及时联系本站,我们会尽快处理。
标题:瑞德西韦临床有效性如何判别? 地址:/news/365.html