929904-85-8
| 中文名 | 瓜地西他钠 |
|---|---|
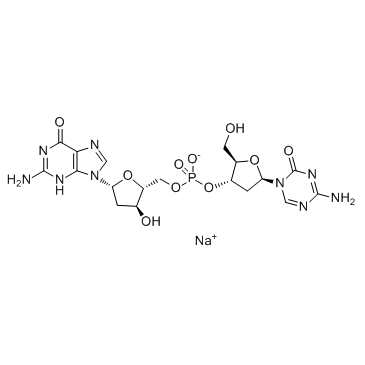
| 英文名 | sodium,[(2R,3S,5R)-5-(2-amino-6-oxo-3H-purin-9-yl)-3-hydroxyoxolan-2-yl]methyl [(2R,3S,5R)-5-(4-amino-2-oxo-1,3,5-triazin-1-yl)-2-(hydroxymethyl)oxolan-3-yl] phosphate |
| 英文别名 |
unii-0rb89yh367
sgi-110 Guadecitabine sodium |
| 描述 | S-110是由5-Aza-CdR和脱氧鸟苷组成的二核苷酸,是有效的DNA甲基化 (DNA methylation inhibitor) 抑制剂。 |
|---|---|
| 相关类别 | |
| 靶点 |
DNMT1 |
| 体外研究 | 在HCT116结肠直肠癌细胞处理6天后,用S-110观察到p16表达的剂量依赖性增加。此外,用S-110或5-aza-CdR处理3天的T24和HCT116细胞显示出p16蛋白水平的剂量依赖性增加,表明S-110抑制DNA甲基化和诱导p16两者的能力。 mRNA和蛋白质水平以及5-aza-CdR。因此,S-110能够抑制5'-区域的DNA甲基化,并以与5-aza-CdR相当的浓度诱导T24和HCT116细胞中p16基因的表达,并且两种药物对p16表达的诱导与之相关。两种细胞系中基因5'末端区域的去甲基化。在高达1μM浓度的测试剂量下,S-110的毒性略低于5-aza-CdR,但在10μM浓度下显示出相似的毒性[1]。 |
| 体内研究 | 10mg/kg的S-110是减少DNA甲基化和延迟肿瘤生长的有效剂量,并且引起与5-Aza-CdR大致相同的毒性水平。 S-110在体内有效地重新激活p16基因的表达,p16基因在亲本EJ6细胞中被严重甲基化。 S-110在降低p16启动子区域的体内DNA甲基化水平方面是有效的。 S-110在体内比5-Aza-CdR具有更好的耐受性,这表明它可能是潜在临床应用的有吸引力的替代品[2]。 |
| 细胞实验 | 将T24细胞以低密度(每60mm培养皿100个)铺板,并用不同浓度的5-aza-CdR和S-110(0.1,0.2,10μM)处理。允许菌落形成10至14天,用甲醇固定,用10%Giemsa染色。未处理对照板的菌落数用于计算每种浓度的平板电镀效率。使用三份培养皿,误差棒用平均值的1 SD表示[ 1]。 |
| 动物实验 | 小鼠:无胸腺nu / nu小鼠在右后腹皮下接种107 EJ6膀胱癌细胞。在肿瘤直径达到0.5cm后,将动物分成三组,每组8只动物开始治疗。设计剂量和给药方案,使得每组接受S-110或5-Aza-CdR的摩尔当量。每周一次给予SQ,S-110剂量为12.2mg / kg,5-Aza-CdR剂量为5.0mg / kg,持续三周。该研究包括适当的PBS对照组。通过卡尺和体重测量的肿瘤大小每周两次,以监测肿瘤生长抑制和耐受性[2]。 |
| 参考文献 |
| 分子式 | C18H23N9NaO10P |
|---|---|
| 分子量 | 579.39300 |
| 精确质量 | 579.12000 |
| PSA | 292.69000 |
| 储存条件 | -20°C,密闭,干燥 |