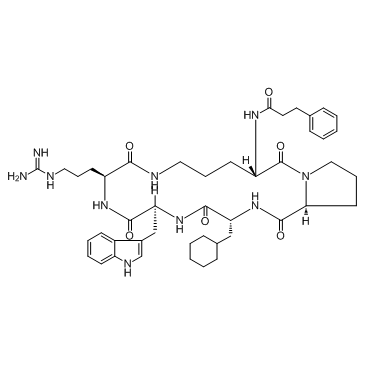
| 描述 |
PMX 205 是一种有效的补体 C5a 受体 (C5aR; CD88) 拮抗剂。
|
| 相关类别 |
|
| 靶点 |
C5aR[1]
|
| 体外研究 |
已知补体激活产物C5a通过激活G蛋白偶联的细胞表面C5aR在体外募集和激活小胶质细胞和星形胶质细胞。在MTT测定中,在24小时平板中,显示与阴性对照组相比所有组均显着。对于PMX 205(PMX205)组,记录的值在0.09893至0.2465,EP54组,0.02724至0.1748和他莫昔芬组之间,记录的值在0.09880至0.2464之间。对于48小时的培养时间,只有两组显示出显着的结果,即PMX 205和他莫昔芬。记录的值分别在0.04987至0.3273和0.5777至0.8551之间。对于72小时平板,只有一组显示出显着的结果,PMX 205(拮抗剂组)的值记录在0.02136至0.5322之间[1]。
|
| 体内研究 |
PMX 205(PMX205)是一种口服活性的选择性C5aR拮抗剂。与媒介物处理的大鼠相比,用PMX 205(1mg/kg /天,口服)治疗的动物显示存活时间的显着延长和终末期运动评分的降低。经PMX205处理的动物在腰脊髓中也显示降低的星形胶质细胞增殖水平。在主要临床症状发作之前的两个时间点(第28天和第70天)口服给予SOD1G93A大鼠PMX205(1mg/kg /天)。与未治疗的大鼠相比,两个治疗组的存活时间均显着延长(p = 0.022,第28天; p = 0.015,第70天),两种治疗方案的结果无明显差异[2]。在12至15个月龄的饮用水(n = 17)中,以20μg/ mL的PMX205(PMX205)处理Tg2576小鼠,这是在这些动物中淀粉样沉积物快速积累的时间范围。未处理的Tg2576动物(n = 11)用作对照。 3个月后,用PMX 205处理的动物显示出比未处理动物显着更少的纤维斑块负荷(硫黄素反应性)。在3×Tg小鼠中,PMX 205也显着降低了过度磷酸化的tau(69%)[3]。
|
| 细胞实验 |
将小鼠乳腺肿瘤细胞系4T1以5.0×10 4细胞/ ml /孔的密度接种在完全培养基中的96-多孔板中。孵育24小时后,用血清饥饿培养基更换培养基以使细胞周期和生长同步,以确保细胞达到其平台期。在血清饥饿24小时后,用5μL/孔的0.1M激动剂,EP54,拮抗剂,PMX205处理细胞,并用他莫昔芬药物处理阳性对照。在读取之前5小时添加5μL/孔的12mM ck溶液,并且添加约50μL/孔的SDS-HCL溶液并在读取之前使用移液管彻底混合3小时。在不同时间点评估MTT测定;使用ELISA板读数器Infinite M200分别在波长570nm处0,24,48和72小时[1]。
|
| 动物实验 |
使用表达人突变体G93A SOD1(NTac:SD-Tg SOD1G93A L26H)的大鼠[2]转基因SOD1G93A大鼠。选择三个实验组:未处理,PMX 205从第28天开始治疗,PMX 205从第70天开始治疗。从第28天或第70天开始,通过饮用水(1mg / kg /天)给动物施用PMX205;控制只接受水[2]。小鼠[3] Tg2576小鼠在饮用水中给予PMX 205治疗(开始于斑块病理学开始或之后)2-3个月(10-20μg/ mL,相当于~3-6 mg / kg)在整个治疗期间,每周两次在饮用水(10-20μg/ mL)和sc(1mg / kg)中两者或两者。未处理的相同年龄的转基因动物用作对照。类似地治疗非转基因同窝小鼠或不用该药物治疗。 3×Tg小鼠也在饮用水中用PMX 205处理。由于雄性的病理学较低,只有这种菌株的雌性小鼠用于这些研究[3]。
|
| 参考文献 |
[1]. Kosni NN, et al. Expression of complement C5a receptor and the viability of 4T1 tumor cells following agonist-antagonist treatment. J Cancer Res Ther. 2016 Apr-Jun;12(2):590-6. [2]. Woodruff TM, et al. The complement factor C5a contributes to pathology in a rat model of amyotrophic lateral sclerosis. J Immunol. 2008 Dec 15;181(12):8727-34. [3]. Fonseca MI, et al. Treatment with a C5aR antagonist decreases pathology and enhances behavioral performance in murine models of Alzheimer's disease. J Immunol. 2009 Jul 15;183(2):1375-83.
|