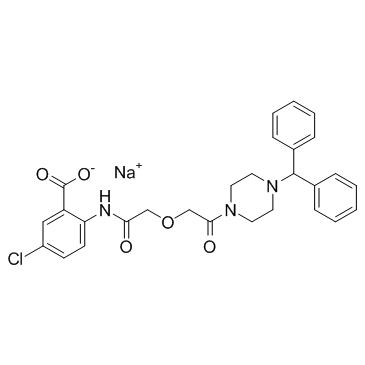
| 描述 |
TM5275 sodium是纤溶酶原激活物抑制剂 (PAI-1),IC50值为6.95 μM。
|
| 相关类别 |
|
| 靶点 |
IC50: 6.95 μM (PAI-1)[1]
|
| 体外研究 |
对接研究表明,TM5275与PAI-1的Aβ-片(s4A)位置的链4结合。 TM5275是一种选择性PAI-1,(高达100μM)不会干扰其他serpin /丝氨酸蛋白酶系统[1]。浓度为20和100μM的TM5275通过抑制tPA-GFP-PAI-1高分子量复合物形成显着延长tPA-GFP在VEC上的保留。 TM5275增强纤溶酶原的时间依赖性积累以及纤维蛋白凝块在tPA-GFP表达细胞上和周围的溶解[2]。在ES-2和JHOC-9细胞中用70-100μMTM5275降低72小时处理的细胞活力。从48小时到96小时,用100μMTM5275抑制细胞生长。与对照处理相比,用100μMTM5275处理的细胞中细胞培养基中的活性PAI-1显着降低。 TM5275被认为在具有高PAI-1表达的卵巢癌中发挥抗增殖作用[3]。
|
| 体内研究 |
TM5275表现出有利的药代动力学特征并且对小鼠和大鼠具有非常低的毒性。在大鼠血栓形成模型中。给予10和50mg/kg TM5275(分别为60.9±3.0和56.8±2.8mg)的大鼠的血凝块重量显着低于载体处理的大鼠(72.5±2.0mg)。 TM5275(50mg/kg)的抗血栓形成效力等于参比抗血栓形成化合物噻氯匹定(500mg/kg)的抗血栓形成效力。在10mg/kg的剂量后,TM5275的血浆浓度达到17.5±5.2μM。 TM5275(5 mg/kg)联合tPA(0.3 mg/kg)可显着增强tPA(0.3 mg/kg)的抗血栓形成作用,并提供与高tPA剂量(3 mg/kg)相似的益处[1] ]。
|
| 激酶实验 |
TM5275表现出有利的药代动力学特征并且对小鼠和大鼠具有非常低的毒性。在大鼠血栓形成模型中。给予10和50mg / kg TM5275(分别为60.9±3.0和56.8±2.8mg)的大鼠的血凝块重量显着低于载体处理的大鼠(72.5±2.0mg)。 TM5275(50mg / kg)的抗血栓形成效力等于参比抗血栓形成化合物噻氯匹定(500mg / kg)的抗血栓形成效力。在10mg / kg的剂量后,TM5275的血浆浓度达到17.5±5.2μM。 TM5275(5 mg / kg)联合tPA(0.3 mg / kg)可显着增强tPA(0.3 mg / kg)的抗血栓形成作用,并提供与高tPA剂量(3 mg / kg)相似的益处[1] ]。
|
| 细胞实验 |
用DMSO(对照)或100μMTM5275处理ES2细胞指定的时间段(24,48,72,96小时)。细胞生长通过CellTiter-Glo测定法确定[1]。
|
| 动物实验 |
大鼠:在雄性CD大鼠中实现动静脉分流中的血栓形成。悬浮于0.5%CMC溶液中的TM5275(10和50mg / kg,n = 9)或噻氯匹定(500mg / kg,n = 6)在研究前90分钟通过管饲口服给药。对照大鼠仅施用0.5%CMC溶液(n = 10)。允许血液通过分流器循环30分钟。最终测量覆盖丝线的血栓的湿重[1]。小鼠:TM5275通过管饲法口服给予雄性ICR小鼠(50mg / kg)。在口服给药之前(0小时)和1,2,6和24小时从静脉收集肝素化的血液样品。血浆药物浓度通过反相高效液相色谱法测定[1]。
|
| 参考文献 |
[1]. Izuhara Y, et al. A novel inhibitor of plasminogen activator inhibitor-1 provides antithrombotic benefits devoid of bleeding effect in nonhuman primates. J Cereb Blood Flow Metab. 2010 May;30(5):904-12. [2]. Yasui H, et al. TM5275 prolongs secreted tissue plasminogen activator retention and enhances fibrinolysis on vascular endothelial cells. Thromb Res. 2013 Jul;132(1):100-5. [3]. Mashiko S, et al. Inhibition of plasminogen activator inhibitor-1 is a potential therapeutic strategy in ovarian cancer. Cancer Biol Ther. 2015;16(2):253-60.
|