Alpelisib (BYL719)
更新时间:2024-01-02 09:47:07
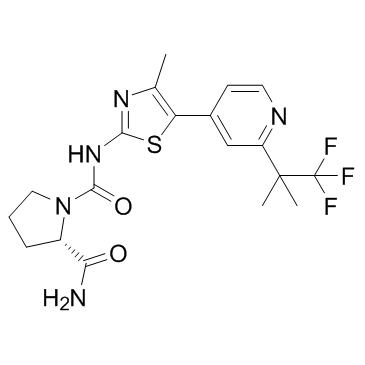
Alpelisib (BYL719)结构式

|
常用名 | Alpelisib (BYL719) | 英文名 | Alpelisib (BYL719) |
|---|---|---|---|---|
| CAS号 | 1217486-61-7 | 分子量 | 441.470 | |
| 密度 | 1.4±0.1 g/cm3 | 沸点 | N/A | |
| 分子式 | C19H22F3N5O2S | 熔点 | N/A | |
| MSDS | N/A | 闪点 | N/A |
Alpelisib (BYL719)用途Alpelisib (BYL-719) 是有效,选择性的 PI3Kα 抑制剂,IC50 为5 nM。 |
| 中文名 | (2S)-N1-[4-甲基-5-[2-(2,2,2-三氟-1,1-二甲基乙基)-4-吡啶]-2-噻唑]-1,2-吡咯烷二羧酰胺 |
|---|---|
| 英文名 | (2S)-1-N-[4-methyl-5-[2-(1,1,1-trifluoro-2-methylpropan-2-yl)pyridin-4-yl]-1,3-thiazol-2-yl]pyrrolidine-1,2-dicarboxamide |
| 中文别名 | 阿吡利塞 |
| 英文别名 | 更多 |
| 描述 | Alpelisib (BYL-719) 是有效,选择性的 PI3Kα 抑制剂,IC50 为5 nM。 |
|---|---|
| 相关类别 | |
| 靶点 |
p110α:5 nM (IC50) p110γ:250 nM (IC50) p110δ:290 nM (IC50) p110β:1200 nM (IC50) |
| 体外研究 | Alpelisib(NVP-BYL719)有效抑制2种最常见的PIK3CA体细胞突变(H1047R,E545K; IC50~4nM)。 Alpelisib(NVP-BYL719)有效抑制PI3Kα转化细胞中的Akt磷酸化(IC50 = 74±15 nM),并显示PI3Kβ或PI3Kδ同种型转化细胞的抑制活性显着降低(与PI3Kα相比≥15倍)[2]。 Alpelisib(NVP-BYL719)通过阻断G0/G1期的细胞周期来减少细胞增殖,对HOS和MOS-J肿瘤细胞中的凋亡细胞死亡没有显着影响。 BYL-719抑制细胞迁移,因此可以被认为是骨肉瘤的细胞抑制药物。在小鼠骨肉瘤的临床前模型中,Alpelisib(NVP-BYL719)显着降低肿瘤进展和肿瘤异位骨形成,如Ki67 +细胞减少和肿瘤血管形成所示。 Alpelisib(NVP-BYL719)在评估的所有细胞系中快速抑制P-AKT和P-mTOR的水平,证实了Alpelisib(NVP-BYL719)对骨肉瘤细胞的功能活性。处理72小时后,Alpelisib(NVP-BYL719)以剂量依赖性方式显着抑制所有骨肉瘤细胞系的细胞生长,IC50范围为6至15μM,IC90为24至42μM,72小时[3]。 |
| 体内研究 | Alpelisib(BYL-719)在大鼠,小鼠和狗中表现出优异的口服生物利用度,并且未显示对CYP450酶的任何显着抑制[1]。 Alpelisib(BYL-719)抑制骨肉瘤的临床前小鼠模型中的肿瘤生长。将具有MOS-J肿瘤的C57Bl/6J(每组n = 6)随机化为对照(载体)或Alpelisib(BYL-719)(12.5mg/kg或50mg/kg每天)[3]。 |
| 细胞实验 | 将两千个肿瘤细胞接种到96孔板中,第二天,用Alpelisib(BYL-719)(1-50μM)处理细胞72小时。使用3'[1-(苯基氨基羰基)-3,4-四唑] - 双(4-甲氧基-6-硝基 - )苯磺酸水合物(XTT试剂测定试剂盒)的比色测定法测定细胞生长/活力。在490nm处读取吸光度。通过台盼蓝排除试验测定细胞活力;在治疗24和48小时后手动计数活细胞和非活细胞[3]。 |
| 动物实验 | 大鼠[2]通过注射3×106至1×10 7个细胞或植入约50mg的肿瘤片段,在裸鼠或裸Rowett大鼠(Hsd:RH-Fox1rnu)中皮下或原位生长肿瘤异种移植物。携带肿瘤的动物小鼠用载体对照,Alpelisib(NVP-BYL719)或NVP-BKM120(po,每天)以所示剂量治疗。对于功效研究,当皮下植入的肿瘤达到约200mm 3并且每天50mg / kg用Alpelisib(NVP-BYL719)治疗时,招募携带肿瘤的动物。报告的反应是治疗最后一天肿瘤体积相对于第0天(治疗开始)的百分比变化。小鼠[3]通过吸入异氟烷/空气混合物(2%,1 L / min)麻醉5周龄雄性C57Bl / 6J小鼠,然后肌肉注射1×106小鼠MOS-J骨肉瘤细胞。到胫骨,导致软组织肿瘤迅速增长,伴有继发性骨质侵入。肿瘤在8天后出现在注射部位并导致成骨细胞损伤,再现成骨细胞形式的人骨肉瘤。随机分配三组(每组n = 6)C57B1 / 6J以接受安慰剂或Alpelisib(BYL719)(口服给药,每日12.5-50mg / kg)。肿瘤细胞接种后1天开始预防性治疗。随机分配4组6个C57Bl / 6J接受安慰剂(口服0.5%甲基纤维素和腹腔注射水),Alpelisib(BYL719)(口服50mg / kg /天),异环磷酰胺(腹腔注射30)在第一周期间三次mg / kg),或Alpelisib(BYL719)(每天50mg / kg)和异环磷酰胺(30mg / kg,第一周三次)的组合。 |
| 参考文献 |
| 密度 | 1.4±0.1 g/cm3 |
|---|---|
| 分子式 | C19H22F3N5O2S |
| 分子量 | 441.470 |
| 精确质量 | 441.144623 |
| PSA | 133.93000 |
| LogP | -0.02 |
| 外观性状 | 粉末 |
| 折射率 | 1.587 |
| 储存条件 | -20℃ |
| Alpelisib (BYL719)上游产品 6 | |
|---|---|
| Alpelisib (BYL719)下游产品 0 | |
| UNII:08W5N2C97Q |
| 1,2-Pyrrolidinedicarboxamide, N-[4-methyl-5-[2-(2,2,2-trifluoro-1,1-dimethylethyl)-4-pyridinyl]-2-thiazolyl]-, (2S)- |
| QCR-1 |
| BYL719 |
| (S)-pyrrolidine-1,2-dicarboxylic acid 2-amide 1-{4-methyl-5-[2-(2,2,2-trifluoro-1,1-dimethyl-ethyl)-pyridin-4-yl]-thiazol-2-yl}amide |
| (2S)-N-{4-Methyl-5-[2-(1,1,1-trifluoro-2-methyl-2-propanyl)-4-pyridinyl]-1,3-thiazol-2-yl}-1,2-pyrrolidinedicarboxamide |
| Alpelisib |
| (2S)-N1 -{4-methyl-5-[1-(1,1,1-trifluoro-2-methylpropan-2-yl)pyridin- 4-yl]-1,3-thiazol-2-yl}pyrrolidine-1,2-dicarboxamide |
| BYL-719 |

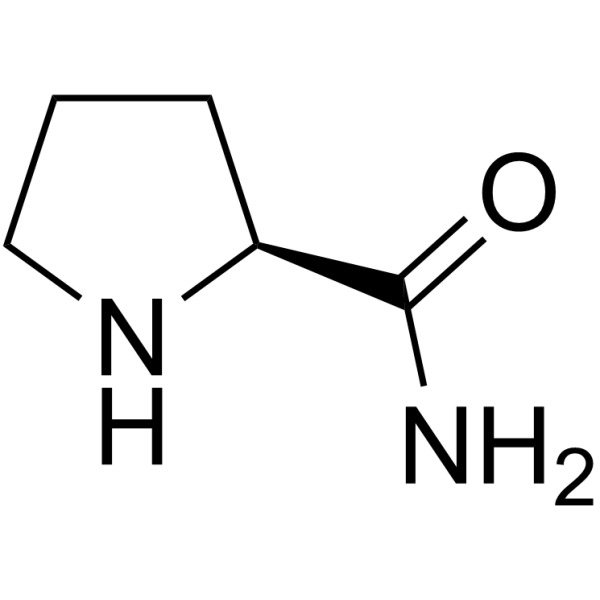 CAS号7531-52-4
CAS号7531-52-4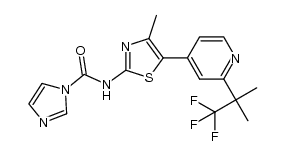 CAS号1357476-70-0
CAS号1357476-70-0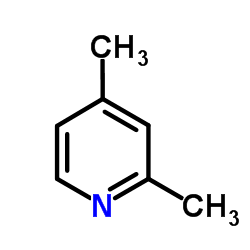 CAS号108-47-4
CAS号108-47-4 CAS号59576-26-0
CAS号59576-26-0 CAS号1378865-93-0
CAS号1378865-93-0 CAS号1396893-42-7
CAS号1396893-42-7
