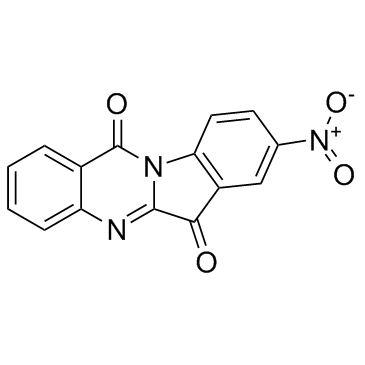
| 描述 |
8-Nitrotryptanthrin 是一种有效的人吲哚胺2,3-双加氧酶 2 (hIDO2) 抑制剂,有效降低 IDO2 活性,Ki 值为 0.97 μM。
|
| 相关类别 |
|
| 靶点 |
rhIDO2:1.8 μM (IC50)
rhIDO2:0.97 μM (Ki)
|
| 体外研究 |
发现八氯氰菊酯衍生物8-硝基十六烷基化物(5i)是一种有效的hIDO2抑制剂,其效率远高于最常用的抑制剂L-1-MT。 IC50值显示所有九种色胺酮化合物均显示出hIDO2抑制活性,尤其是化合物8-硝基转染素显示出比L-1-MT(82.53μM)和D-1-MT(262.75μM)更强的抑制作用(1.87μM)。 。 8-硝基转化长素具有显着的抗锥体活性,EC50为0.82μM[2]。 8-硝基转化染素具有微孔板Alamar Blue测定(MABA)的最小抑制浓度(MIC)值为0.032μg/ mL。 8-Nitrotryptanthrin的LORA MIC值也为2.4μg/ mL,而大多数类似物缺乏LORA活性[3]。
|
| 激酶实验 |
IDO2的色氨酸分解代谢活性和酶动力学特性具有轻微改变的特征。与IDO1类似,IDO2也易于自动氧化。在此,为了维持酶活性,在生物测定系统中补充抗坏血酸(还原剂),亚甲蓝(电子载体)和过氧化氢酶(以避免H2O2对IDO2的抑制)。为了筛选IDO2抑制剂候选物,将每种组分溶解在pH7.5的50mM磷酸钾缓冲液中。每种测定溶液含有500μL反应混合物,其包含40mM抗坏血酸,200μg/ mL过氧化氢酶,20μM亚甲基蓝,底物L-色氨酸(0-40mM),抑制剂候选物(10μM用于初步筛选和适当的浓度梯度,用于Ki和IC50值测定)和最终浓度为1500nM的酶。在恒温控制的水浴中在37℃下进行测定30分钟,并通过加入200μL三氯乙酸(30%w / v)终止测定。为了促进L-犬尿氨酸的形成,在65℃下在水浴中进行另外的孵育15分钟。每个反应一式三份进行。在13,000×g,4℃下离心15分钟后,将100μL来自每个管的上清液转移到96孔微量培养板中并与等体积的4-二甲基氨基苯甲醛(DMAB)在乙酸中混合(2%w / v)。由IDO2催化的L-Trp的双氧化产生的测定产物通过测量它们在492nm处的吸光度来确认,在该波长处,犬尿氨酸-DMAB复合物具有吸收峰。在测定中,包括对照以消除干扰,例如在不存在IDO2的情况下抑制剂分子与底物或具有DMAB的底物的任何反应。为了筛选IDO2抑制剂,在与对照相同的条件下测量典型竞争性抑制剂L-1-MT和D-1-MT的抑制活性[1]。
|
| 细胞实验 |
为了研究细胞hIDO2对候选化合物的抑制作用,构建了重组质粒pcDNA3.1(+) - hIDO2,并将其转染到没有IDO1表达的人胶质母细胞瘤U87 MG细胞中(通过RT-PCR和western blot证实),从而消除了干扰。 IDO1。 U87 MG细胞在含有50U / mL青霉素,50mg / mL链霉素,4500mg / L葡萄糖和10%灭活FBS的DMEM中在37℃,5%CO 2和95%湿度下培养。当达到80%汇合单层的细胞密度时,使用转染试剂Lipofectamine 2000根据制造商的说明用pcDNA3.1(+) - hIDO2转染U87 MG细胞。空pcDNA3.1(+)表达载体用作对照。温育18小时后,将转染的细胞以2.5×10 4个细胞/孔的密度接种在96孔培养板中,最终体积为200μL,补充有200μML-Trp。在另外6小时的温育后,将测试化合物的连续稀释液加入培养基中。 24小时后,通过加入30%(w / v)三氯乙酸(10μL,140μL反应混合物)终止反应。将板在65℃下在水浴中温育15分钟以促进N-甲酰基犬尿氨酸转化为L-犬尿氨酸,然后以13,000×g离心10分钟以除去沉淀物。然后将100μL上清液转移到另一个96孔板中,并与相同体积的2%(w / v)4-二甲基氨基苯甲醛的乙酸溶液混合。通过使用酶标仪测量492nm处的吸光度来计算化合物对色氨酸降解或犬尿氨酸产生的抑制百分比。使用GraphPad Prism 5.0 [1]通过非线性回归分析确定细胞IC50。
|
| 参考文献 |
[1]. Li J, et al. Establishment of a human indoleamine 2, 3-dioxygenase 2 (hIDO2) bioassay system and discovery of tryptanthrin derivatives as potent hIDO2 inhibitors. Eur J Med Chem. 2016 Nov 10;123:171-9. [2]. Scovill J, et al. Antitrypanosomal activities of tryptanthrins. Antimicrob Agents Chemother. 2002 Mar;46(3):882-3. [3]. Hwang JM, et al. Design, synthesis, and structure-activity relationship studies of tryptanthrins as antitubercular agents. J Nat Prod. 2013 Mar 22;76(3):354-67.
|