1004997-71-0
| 中文名 | CR4056 |
|---|---|
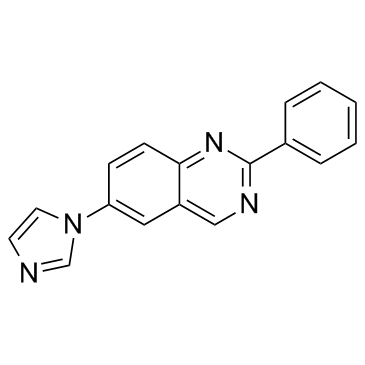
| 英文名 | 6-(1H-Imidazol-1-yl)-2-phenylquinazoline |
| 英文别名 |
Quinazoline, 6-(1H-imidazol-1-yl)-2-phenyl-
6-(1H-Imidazol-1-yl)-2-phenylquinazoline CR4056 |
| 描述 | CR4056 是一个选择性的人重组 MAO-A 抑制剂,其 IC50 值为 202.7 nM。 CR4056 也是咪唑啉-2 受体 (I2R) 的配体,其 IC50 值为 596 nM。 |
|---|---|
| 相关类别 | |
| 靶点 |
IC50: 202.7 nM (MAO-A), 596 nM (I2R)[1] |
| 体外研究 | CR4056是咪唑啉-2受体(I2R)配体,IC50为596±76nM。 CR4056也是人重组MAO-A和MAO-B的抑制剂,IC50分别为202.7±10.3和> 10000 [1]。在所有使用浓度(范围3至30μM)下硼替佐米(BTZ)与CR4056的联合治疗与BTZ处理的细胞相比,在H929或RPMI 8226骨髓瘤细胞中均不会导致细胞存活率的任何显着差异[2] ]。 |
| 体内研究 | 单次口服20mg/kg CR4056后2小时,内源性去甲肾上腺素(NE)水平在枕叶皮质中增加68.2%±14.1%(与载体相比P <0.05)。每日一次20 mg/kg CR4056的亚慢性(4天)口服治疗,显着增加大脑皮质(63.1%±4.2%; P <0.05与媒介物)和腰脊髓(51.3%±)的NE水平6.7%;与载体相比P <0.05。 CR4056剂量依赖性地减少机械痛觉过敏(有效剂量[ED50] = 5.8mg/kg)(P <0.001)。 CR4056(10mg/kg)和吡罗昔康(10mg/kg)显着逆转由辣椒素引起的戒断阈值的降低(与媒介物相比P <0.001)。 CR4056的最高测试剂量(30mg/kg)完全逆转辣椒素的作用,1小时后爪缩回阈值(PWT)增加至239±12g(与载体相比P <0.001)。 CR4056剂量依赖性地降低链脲佐菌素(STZ)诱导的大鼠糖尿病疼痛(F [4,35] = 31.27,P <0.001)。与车辆对照相比,CR4056显着增加了同侧(F [4,30] = 19.97,P <0.001)和对侧(F [4,30] = 31.58,P <0.001)后爪的机械退缩阈值[1]。 |
| 激酶实验 | 对大鼠大脑皮质膜中的单胺氧化酶进行结合测定。总之,对于MAO-A结合测定,氚化的N-(2-氨基乙基)-5-(间 - 氟苯基)-4-噻唑甲酰胺HCl([3H] Ro 41-1049,10nM)在不存在的情况下孵育或存在CR4056在37℃下60分钟,并且在1μMclorgyline存在下测定非特异性结合。对于MAO-B结合测定,[3H] Ro 19-6327(氚化的lazabemide)(15nM)的温育在22℃下进行90分钟,并且在10μM(R)存在下测定非特异性结合。 -deprenyl [1]。 |
| 细胞实验 | 为了排除CR4056与硼替佐米(BTZ)诱导的细胞毒性的任何干扰,用BTZ和CR4056同时处理非小细胞肺癌和MM细胞系72小时。在细胞毒性研究中估计细胞暴露于BTZ的IC50,有或没有三种浓度的CR4056(3,10和30μM)。还进行了与CR4056单独(3,10和30μM)和最高剂量的载体(DMSO)的孵育。通过MTT测定评估生长抑制。在这些实验中,CR4056在体外测试的浓度范围从药理学到毒理学水平[2]。 |
| 动物实验 | 大鼠:在给药前将大鼠禁食过夜。在注射辣椒素之前进行疼痛阈值的第一次测量。辣椒素在时间t = 0时通过右后爪的足底内途径给予(10μL的1mg / mL吐温80 /盐水溶液)。 60分钟后,通过口服途径给予动物CR4056(3至30mg / kg)或其载体,体积为5mL / kg。假对照组始终存在以进行比较。在机械研究中,拮抗剂在辣椒素后30分钟和CR4056给药前15分钟给药[1]。 |
| 参考文献 |
| 密度 | 1.3±0.1 g/cm3 |
|---|---|
| 沸点 | 364.1±24.0 °C at 760 mmHg |
| 分子式 | C17H12N4 |
| 分子量 | 272.304 |
| 闪点 | 174.0±22.9 °C |
| 精确质量 | 272.106201 |
| LogP | 3.09 |
| 蒸汽压 | 0.0±0.8 mmHg at 25°C |
| 折射率 | 1.699 |
| 储存条件 | 2-8℃ |