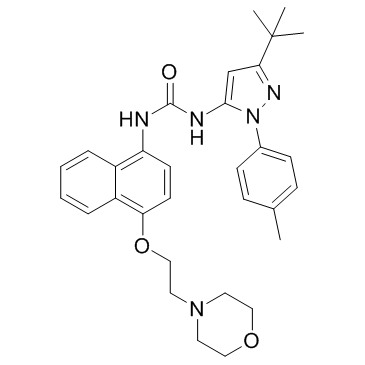
285983-48-4
| 中文名 | 1-[2-(4-甲基苯基)-5-叔丁基吡唑-3-基]-3-[4-(2-吗啉-4-基乙氧基)萘-1-基]脲 |
|---|---|
| 英文名 | 1-[5-tert-butyl-2-(4-methylphenyl)pyrazol-3-yl]-3-[4-(2-morpholin-4-ylethoxy)naphthalen-1-yl]urea |
| 中文别名 |
脲,N-[3-(1,1-二甲基乙基)-1-(4-甲基苯基)-1H-吡唑-5-基]-N'-[4-[2-(4-吗啉基)乙氧基]-1-萘基]
多马莫德 达马莫德 |
| 英文别名 |
1kv2
BIRB796 1-[3-tert-Butyl-1-(4-methylphenyl)-1H-pyrazol-5-yl]-3-{4-[2-(morpholin-4-yl)ethoxy]-1-naphthyl}urea S1574_Selleck Kinome_2137 1-(3-tert-butyl-1-p-tolyl-1H-pyrazol-5-yl)-3-(4-(2-morpholinoethoxy)naphthalen-1-yl)urea L66J BO2- AT6N DOTJ& EMVM- ET5NNJ AR D1& CX1&1&1 doramapimod Urea, N-[3-(1,1-dimethylethyl)-1-(4-methylphenyl)-1H-pyrazol-5-yl]-N'-[4-[2-(4-morpholinyl)ethoxy]-1-naphthalenyl]- 1-[1-(4-Methylphenyl)-3-(2-methyl-2-propanyl)-1H-pyrazol-5-yl]-3-{4-[2-(4-morpholinyl)ethoxy]-1-naphthyl}urea BIRB 796 UNII-HO1A8B3YVV |
| 描述 | Doramapimod 是一种高效的 p38α 抑制剂,IC50 为 4 nM,也抑制 B-Raf 和 Abl,IC50 分别为 83 nM 和 14.6 μM。 |
|---|---|
| 相关类别 | |
| 靶点 |
B-Raf:83.4 nM (IC50) p38α:4 nM (IC50) Abl:14600 nM (IC50) |
| 体外研究 | Doramapimod(BIRB 796)是一种高效的p38α抑制剂,一种丝氨酸/苏氨酸丝裂原活化蛋白激酶(MAPK),由于其在T细胞增殖和细胞因子产生中的作用,通常与炎症相关[1]。 Doramapimod(BIRB 796)是人p38 MAP激酶的皮摩尔抑制剂[2]。在用山梨糖醇刺激(渗透压休克)之前,将HEK293细胞与不同浓度的Doramapimod(BIRB 796)孵育30分钟或2小时,并通过测量其活性检查MAPKAP-K2的活化。 MAPKAP-K2活化在这些细胞中以时间依赖性方式被抑制,30分钟后表观IC50为30 nM或与Doramapimod预培养2小时后8 nM [3]。 |
| 体内研究 | Doramapimod(BIRB 796)加紫杉醇组(1.14±0.48 g)的平均异种移植重量轻于对照,Doramapimod或紫杉醇组(1.84±0.61,1.80±0.62和1.65±0.29 g)(P <0.05)在Athymic裸体中小鼠(BALB/c-nu/nu)。 Doramapimod,紫杉醇和Doramapimod加紫杉醇的抑制率分别为1.93%,9.93%和38%。重要的是,与对照组,紫杉醇或单独的Doramapimod相比,Doramapimod和紫杉醇的组合可显着抑制肿瘤生长[4]。 Doramapimod(BIRB 796)治疗略微降低血压(第7周166±7 mm Hg; P <0.05),而SD大鼠血压正常(123±3 mm Hg)。尽管血压降低,未治疗和Doramapimod治疗的dTGR具有相似的心脏重量和心脏肥大指数(心脏-胫骨比),与非转基因SD大鼠相比显着更高(310±6对307±6对比206±分别为5 mg/cm; P <0.05)[5]。 |
| 激酶实验 | 在含有20mM Bis-Tris丙烷,pH 7.0,2mM EDTA,0.01%(w / v)NaN 3和0.15%(w / v)正辛基葡糖苷的缓冲液中进行结合研究。在配备有停止流量控制器的Kintech荧光检测器系统上收集SK&F 86002与p38 MAP激酶结合的动力学数据。数据同时适合描述动态结合的适当方程式,用于简单的一步结合机制。针对未结合配体的背景荧光校正BIRB 796的荧光类似物结合的数据。使用SLM Aminco Bowman Series 2 Model SQ-340荧光检测器将交换曲线测定作为两个半反应进行。在第一个半反应中,将p38 MAP激酶和SK&F 86002预孵育3分钟。在第二个半反应中,将p38 MAP激酶与Doramapimod预孵育60分钟。对于第一次半反应,观察到荧光探针的净离解,并且观察到第二次半反应的净关联。来自两个半反应的原始数据同时适合描述简单竞争抑制的等式。通过用组成型活性重组MKK6(通过将两个活化残基Ser189和Thr193诱变为Glu残基制备)预处理p38。纯化活化的p38并用作标准激酶活性测定中的酶来源,监测放射性磷酸盐掺入重组人MAPKAP k2中。细胞试验遵循公开的程序。简言之,在存在或不存在化合物的情况下,用1μg/ mL LPS刺激人THP.1细胞,然后使用商业ELISA kitkinase测定释放的TNF [2]。 |
| 细胞实验 | 将人胚肾(HEK)293和HeLa细胞暴露于0.5M山梨糖醇30分钟或100ng / mL EGF 10分钟,然后在缓冲液A(50mM Tris-HCl,pH7.5,1mM EGTA,1mM)中裂解。 EDTA,1 mM原钒酸钠,10 mM氟化钠,50 mMβ-甘油磷酸钠,5 mM焦磷酸盐,0.27 M蔗糖,0.1 mM苯甲基磺酰氟,1%(v / v)Triton X-100)加0.1%(v / v)2-巯基乙醇和完全蛋白酶抑制剂混合物。将裂解物在4℃下以18,000×g离心5分钟,除去上清液,在液氮中快速冷冻,并在-20℃下储存直至使用。需要时,将细胞在没有或不含10μMSB203580或10μMPD184352或不同浓度的Doramapimod的情况下预培养1小时,持续时间如图[3]所示。 |
| 动物实验 | 使用小鼠[4]无胸腺裸鼠(BALB / c-nu / nu),6至8周龄,体重18至24g。在该研究中使用KBV200接种的裸鼠异种移植模型。简而言之,将收获的KBV200细胞(2×10 7个细胞/0.2mL /小鼠)皮下植入裸鼠的肩部。当肿瘤达到平均直径0.5 cm3时,将小鼠随机分成4组,并用以下方案治疗:1)盐水溶液(每3天×5); 2)紫杉醇(18mg / kg ip,每3天×5); 3)Doramapimod(10mg / kg po,每3天×5); 4)紫杉醇(18mg / kg ip,每3天×5)加Doramapimod(10mg / kg po,每3天×5,在注射紫杉醇前1小时给药)。每3天记录动物的体重和两个垂直肿瘤直径(A和B),并根据下式估算肿瘤体积(V):V =(π/ 6)[(A + B) )/ 2] 3。根据肿瘤体积和植入时间绘制肿瘤生长和体重的曲线。当对照组中的平均肿瘤重量超过1g时,将小鼠麻醉并杀死。从小鼠切下肿瘤组织,测量它们的重量。生长抑制率(IR)根据下式计算:IR = [1-(实验组的平均肿瘤重量/对照组的平均肿瘤重量)]×100%。大鼠[5]使用雄性转基因dTGR(RCC Ltd)和年龄匹配的非转基因Sprague-Dawley(SD)大鼠(MDC)。执行2种不同的协议。在方案2中,分析未处理的dTGR(n = 15),dTGR + BIRB796(饮食中每天30mg / kg,持续3周; n = 11)和SD(每组n = 8)。通过尾套每周测量收缩压。从第5周到第7周在代谢笼中收集二十四小时的尿样。在第7周收集血清。通过临床常规测定测量血清肌酸酐和胱抑素C.通过酶联免疫吸附测定法测定尿大鼠白蛋白。方案2的目的是关注电生理学改变和死亡率。研究未治疗的dTGR(n = 10),dTGR + BIRB796(n = 10)和SD(n = 10)大鼠至第8周。在异氟烷麻醉下在第7周进行心脏磁场作图(CMFM)。进行超声心动图检查。 |
| 参考文献 |
| 密度 | 1.2±0.1 g/cm3 |
|---|---|
| 沸点 | 631.6±55.0 °C at 760 mmHg |
| 分子式 | C31H37N5O3 |
| 分子量 | 527.657 |
| 闪点 | 335.8±31.5 °C |
| 精确质量 | 527.289612 |
| PSA | 80.65000 |
| LogP | 6.11 |
| 蒸汽压 | 0.0±1.9 mmHg at 25°C |
| 折射率 | 1.620 |
| 储存条件 | -20°C |