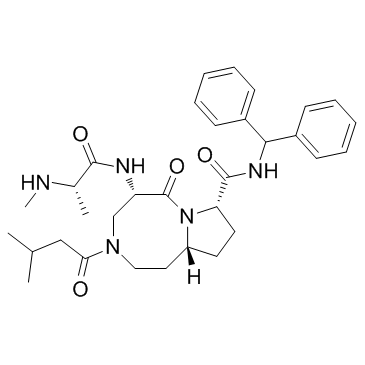
| 描述 |
AT-406 是一种有效的,可口服的 Smac 模拟物,为 IAPs 的拮抗剂,能够抑制 XIAP,cIAP1 和 cIAP2 蛋白,Ki 值分别为 66.4,1.9 和 5.1 nM。
|
| 相关类别 |
|
| 靶点 |
Ki: 66.4 nM (XIAP), 1.9 nM (cIAP1), 5.1 nM (cIAP2)
|
| 体外研究 |
AT-406在与XIAP的氢键和疏水相互作用中模拟AVPI肽,与XIAP的W323具有额外的疏水接触。 AT-406对这些IAP比对Smac AVPI肽更敏感,具有50-100倍的结合亲和力。 AT-406(1μM)完全恢复caspase-9的活性,其在无细胞系统中被500nM XIAP BIR3抑制。在MDA-MB-231细胞中,AT-406诱导快速细胞cIAP1降解并且还降低细胞XIAP蛋白。 AT-406有效抑制大量人类癌细胞系,在MDA-MB-231细胞和SK-OV-3卵巢细胞中IC50分别为144和142 nM,对正常样人乳腺上皮MCF-12F细胞具有低毒性,原发性人正常前列腺上皮细胞。 AT-406通过诱导caspase-3的激活和PARP的裂解诱导MDA-MB-231细胞凋亡[1]。 AT-406在卵巢癌细胞系中显示单一药剂活性。这些卵巢癌细胞中AT-406的IC 50值为0.05-0.5μg/ mL。 AT-406作为单一药剂和与卡铂组合显示出抗卵巢癌功效。 AT-406(30μg/ mL)诱导药物敏感性卵巢癌细胞系中XIAP的降解[2]。
|
| 体内研究 |
AT-406在小鼠,大鼠,非人灵长类动物和狗中具有良好的药代动力学特性和口服生物利用度。在MDA-MB-231异种移植物中,AT-406有效诱导cIAP1降解和procaspase-8的加工,以100mg/kg切割肿瘤组织中的PARP,即使在200mg/kg时也具有良好的耐受性。 AT-406诱导显着的肿瘤生长抑制,p为0.0012,100 mg/kg [2]。 SM-406(30,100 mg/kg,po)可降低荷瘤小鼠的血浆和肿瘤[3]。
|
| 激酶实验 |
通过将细胞溶解于含有KCl(50mM),EGTA(5mM),MgCl 2(2mM)DTT(1mM),0.2%CHAPS和HEPES(50mM,50mM)的冰冷缓冲液中来制备MDA-MB-231细胞裂解物。 pH 7.5),含有鸡尾酒蛋白酶抑制剂,在冰上孵育10分钟,然后在液氮中冷冻。将细胞色素c和dATP加入细胞裂解物中,然后将其在30℃水浴中孵育60分钟以活化胱天蛋白酶-9。重组XIAP BIR3蛋白的添加剂量依赖性地抑制胱天蛋白酶-9的活性。加入不同浓度的测试Smac模拟物(1nM-100μM)以确定这些半胱天冬酶活性的恢复。
|
| 细胞实验 |
将细胞以3-4×103个细胞/孔的密度接种在96孔平底细胞培养板中,用AT-406培养4天。用不同浓度的AT-406处理后细胞生长抑制率通过(2-(2-甲氧基-4-硝基苯基)-3-(4-硝基苯基)-5-(2,4-二磺基苯基))测定来确定-2H-四唑鎓单钠盐(WST-8)。在每个孔中加入WST-8至终浓度为10%,然后将板在37℃下孵育2-3小时。样品的吸光度为使用TECAN ULTRA读数器在450nm处测量。通过比较未处理细胞和用AT-406处理的细胞的吸光度来计算抑制细胞生长50%的IC-406浓度(IC 50)。
|
| 动物实验 |
携带MDA-MB-231异种移植肿瘤的SCID小鼠(每组8-10个)用不同剂量的化合物2或7.5mg / kg Taxotere或载体对照每天,每周5天,持续2周。在治疗期间每周测量3次肿瘤大小和动物重量,在治疗后每周测量两次。数据表示为平均肿瘤体积±SEM。使用Prism通过双向ANOVA和非配对双尾t检验进行统计学分析。 P <0.05被认为具有统计学意义。
|
| 参考文献 |
[1]. Cai Q, et al. A potent and orally active antagonist (SM-406/AT-406) of multiple inhibitor of apoptosis proteins (IAPs) in clinical development for cancer treatment. J Med Chem. 2011 Apr 28;54(8):2714-26. [2]. Brunckhorst MK, et al. AT-406, an orally active antagonist of multiple inhibitor of apoptosis proteins, inhibits progression of human ovarian cancer. Cancer Biol Ther. 2012 Jul;13(9):804-11. [3]. Zhang T, et al. Physiologically based pharmacokinetic and pharmacodynamic modeling of an antagonist (SM-406/AT-406) of multiple inhibitor of apoptosis proteins (IAPs) in a mouse xenograft model of human breast cancer. Biopharm Drug Dispos. 2013 Sep;34(6):
|