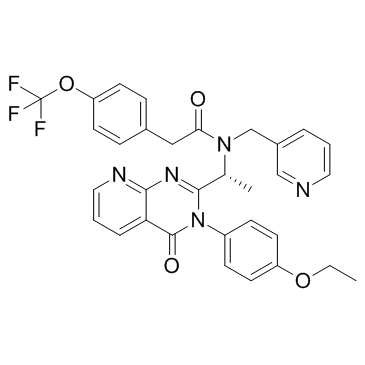
473719-41-4
| 中文名 | AMG-487 |
|---|---|
| 英文名 | amg 487 |
| 英文别名 |
Benzeneacetamide, N-((1R)-1-(3-(4-ethoxyphenyl)-3,4-dihydro-4-oxopyrido[2,3-d]pyrimidin-2-yl)ethyl)-N-(3-pyridinylmethyl)-4-(trifluoromethoxy)-
N-[(1R)-1-[3-(4-ethoxyphenyl)-4-oxopyrido[2,3-d]pyrimidin-2-yl]ethyl]-N-(pyridin-3-ylmethyl)-2-[4-(trifluoromethoxy)phenyl]acetamide |
| 描述 | AMG 487 是一种有效的趋化因子受体3 (CXCR3) 拮抗剂,抑制 CXCL10和 CXCL11与 CXCR3 结合的 IC50 值分别为 8.0 和 8.2 nM。 |
|---|---|
| 相关类别 | |
| 靶点 |
125I-IP10-CXCR3:8 nM (IC50) 125I-ITAC-CXCR3:8.2 nM (IC50) |
| 体外研究 | AMG 487通过三种CXCR3趋化因子抑制CXCR3介导的细胞迁移(IP-10 IC 50 = 8nM,ITAC IC 50 = 15nM,MIG IC 50 = 36nM)。此外,AMG 487抑制响应ITAC的钙动员(IC50 = 5 nM)[1]。 AMG487(1μM)发展为肺转移较少,肺部明显小于载体治疗的肺[2]。 AMG487消除了C26肿瘤细胞的增殖/存活[3]。 |
| 体内研究 | AMG 487(0.03-10 mg/kg,sc)以剂量依赖的方式表现出细胞向肺部的浸润显着减少[1]。 AMG487(5 mg/kg,sc,每日两次)转移的转移率低于载体治疗的小鼠[2]。在两种模型中,AMG487(5mg/kg,sc)处理的小鼠表现出比对照小鼠更少的肺结节。 AMG487可降低肿瘤体积[3]。 |
| 激酶实验 | 然后裂解细胞并在50mM Hepes pH 7.5,150mM NaCl,20mM EDTA,1mM PMSF,10μg/ mL亮肽素,2μg/ mL抑肽酶和0.2%NP-40中超声处理。将等量的裂解物在基质缓冲液(50mM Hepes,100mM NaCl,1mM EDTA,10%蔗糖,0.5%CHAPS,5mM二硫苏糖醇)中与Ac-DEVD-AMC底物和半胱天冬酶-3/7底物混合。微量滴定板。在37℃下在分光光度计Ascent Fluoroskan中连续测量荧光底物的产生,并且半胱天冬酶活性(表示为U / mg蛋白质)定义为酶切割1nmol底物/ min的量。 |
| 细胞实验 | 将结肠癌细胞以104细胞cm2的密度接种,并在富含血清的培养基中或在含有或不含有各种浓度的rCXCL9,rCXCL10和rCXCL11的基础培养基(含有0.1%牛血清白蛋白,BSA)中孵育指定的时期在用胰蛋白酶分离,收集和计数或用新鲜培养基重新喂养3天之前的时间,收获和计数。通过倒置光学显微镜在×20放大倍数下观察CRC细胞的形态,并在第7天拍摄照片。 |
| 动物实验 | 通过在同源雌性小鼠的右腹乳腺附近注射3×105个活肿瘤细胞来评估局部肿瘤生长和自发转移。通过卡尺每周两次测量肿瘤直径,并且当sc肿瘤测量直径18mm或更早时如果小鼠看起来垂死,则对个体进行小鼠安乐死。取出肺并称重,并在解剖显微镜下以盲法定量表面肿瘤集落。通过将9×104个存活的肿瘤细胞静脉注射到同系雌性小鼠的侧尾静脉中来评估实验性转移。如果小鼠看起来垂死,则在移植后第21天或更早时对所有小鼠实施安乐死。取出肺并称重,并在解剖显微镜下以盲法定量表面肿瘤集落。制备50%羟丙基-β-环糊精溶液;在20%时,该解决方案用作车辆。将AMG487加入到50%溶液中,并将其在超声水浴中温育2小时,偶尔涡旋。加入蒸馏水,在20%羟丙基-β-环糊精中得到适当的AMG487终浓度。 |
| 参考文献 |
| 分子式 | C32H28F3N5O4 |
|---|---|
| 分子量 | 603.59100 |
| 精确质量 | 603.20900 |
| PSA | 99.44000 |
| LogP | 5.80550 |
| 储存条件 | 2-8℃ |