| 描述 |
Bendamustine (SDX-105 free base),一种嘌呤类似物,是一种 DNA 交联剂。Bendamustine 可激活 DNA 损伤反应和细胞凋亡 (apoptosis)。Bendamustine 具有有效的烷基化,抗癌和抗代谢作用。
|
| 相关类别 |
|
| 靶点 |
DNA Alkylator/Crosslinker[1]
|
| 体外研究 |
苯达莫司汀是一种能引起DNA断裂的DNA交联剂,具有烷基化和抗代谢特性。苯达莫司汀独特调节非霍奇金淋巴瘤细胞凋亡途径和DNA修复途径。苯达莫司汀(50μM)诱导p21(Cip1/Waf1)和NOXA基因,增加SU-DHL-1细胞p53的表达。有丝分裂阻滞(25μcuustic)。苯达莫司汀降低多发性骨髓瘤细胞系,如RPMI-8226和8226-LR5细胞,培养24小时后ic25分别为101.8μM和585.5μM,48h后分别为51.7和374.3μM。苯达莫司汀诱导特异性caspase依赖性MM细胞死亡并抑制纺锤体组装检查点[2]。
|
| 体内研究 |
苯达莫司汀(25mg/kg,i.v.)对DoHH-2、Granta 519和RAMOS模型的肿瘤细胞生长抑制率分别为91%、99%和95%。此外,利妥昔单抗在DoHH-2和RAMOS模型中增强了苯达莫司汀的抗肿瘤作用,但在Granta 519模型中没有增强[3]。
|
| 细胞实验 |
本达莫司汀和美法仑对多发性骨髓瘤(MM)细胞的细胞毒性是通过MTS测定细胞存活率来计算的。简单地说,细胞(1×104/孔)接种在96孔板中,培养24、48、72和96小时后进行分析。为此,向每个孔中添加1μg/mL的MTS溶液,并在37°C下1 h后,用异丙醇1 N和HCl(24:1,体积/体积)溶解深蓝色甲氧杂氮晶体。最后,在96孔板读卡器中,在490nm处测量吸光度。细胞存活率估计为未经处理对照品吸光度的百分比,每次试验一式三份。计算每种药物的抑制浓度50(IC50)和25(IC25),即能够将细胞生长分别降低到未处理对照细胞的50%和25%的量,并使用等毒性浓度的苯达莫司汀和美法仑平行进行试验。相对抗性指数(RRI)表示为8226-LR5细胞的IC50与RPMI-8226细胞的IC50之比[2]。
|
| 动物实验 |
小鼠[3]C.B.-17 scid小鼠(DoHH-2,Granta 519)或C.B.-17 scid-bg小鼠(SuDHL-4,RAMOS)在右侧接种1×106(DoHH-2,RAMOS)、3×106(SuDHL-4)或5×106(Granta 519)细胞。侧翼异种移植,接种量为0.2ml,由生长培养基和基质凝胶中细胞的50:50混合组成。肿瘤体积通过两到三周用电子卡尺测量肿瘤的长度和宽度来估计,并应用以下公式:V=L×W2/2。肿瘤可以达到大约250 mm3,并且小鼠大小匹配(第0天)进入治疗组和对照组。对于全身性Granta 519肿瘤模型,在第0天通过尾静脉注射2×106细胞于0.1 mL体积的细胞培养基中,并在第14天开始治疗。在整个实验过程中,所有的动物都被贴上了耳朵标签,并被单独监控。Navitoclax每日口服灌胃给药,以50PG:PEG400:乙醇的混合物灌胃给药。在第1天静脉注射苯达莫司汀和利妥昔单抗,剂量分别为25 mg/kg和10 mg/kg。在本达莫司汀和利妥昔单抗前约2小时给予纳维克拉。所有试验由每组10只小鼠组成。当肿瘤体积大于2000mm3或监测到任何痛苦迹象时,都会人道地杀死老鼠。痛苦的迹象包括失去活动能力、呼吸困难或体重下降>每个笼子平均体重的20%[3]。
|
| 参考文献 |
[1]. Leoni LM, et al. Bendamustine (Treanda) displays a distinct pattern of cytotoxicity and unique mechanistic features compared with other alkylating agents. Clin Cancer Res. 2008 Jan 1;14(1):309-17. [2]. Cives M, et al. Bendamustine overcomes resistance to melphalan in myeloma cell lines by inducing cell death through mitotic catastrophe. Cell Signal. 2013 May;25(5):1108-17. [3]. Ackler S, et al. Navitoclax (ABT-263) and bendamustine ± rituximab induce enhanced killing of non-Hodgkin's lymphoma tumours in vivo. Br J Pharmacol. 2012 Oct;167(4):881-91.
|



![5-[双(2-羟乙基)氨基]-1-甲基-1H-苯并咪唑-2-丁酸乙酯结构式](https://image.chemsrc.com/caspic/370/3543-74-6.png) CAS号3543-74-6
CAS号3543-74-6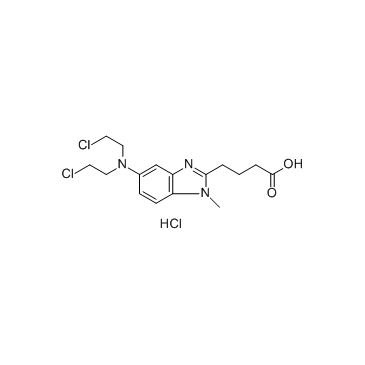 CAS号3543-75-7
CAS号3543-75-7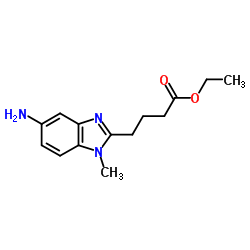 CAS号3543-73-5
CAS号3543-73-5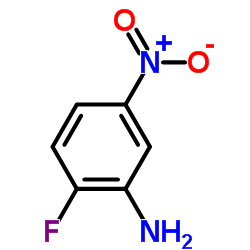 CAS号369-36-8
CAS号369-36-8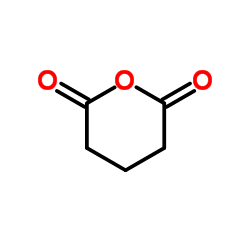 CAS号108-55-4
CAS号108-55-4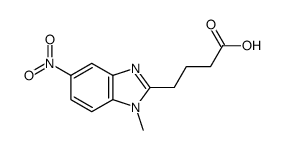 CAS号31349-48-1
CAS号31349-48-1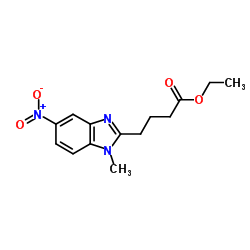 CAS号3543-72-4
CAS号3543-72-4![5-[双(2-氯乙基)氨基]-1-甲基-1H-苯并咪唑-2-丁酸甲基酯结构式](https://image.chemsrc.com/caspic/156/109882-25-9.png) CAS号109882-25-9
CAS号109882-25-9
